Tecniche avanzate di microingegneria per creare un modello miniaturizzato in vitro del processo di differenziamento e rigenerazione muscolare per testare le strategie terapeutiche per la DMD. Su questa tecnologia innovativa si è basato uno studio italiano per valutare l’efficacia della terapia cellulare con mesoangioblasti. Un approccio che apre nuove interessanti prospettive per lo sviluppo dei futuri studi clinici.
di Francesca Ceradini
Riuscire a ripristinare un’adeguata produzione di distrofina nelle cellule muscolari è uno dei principali 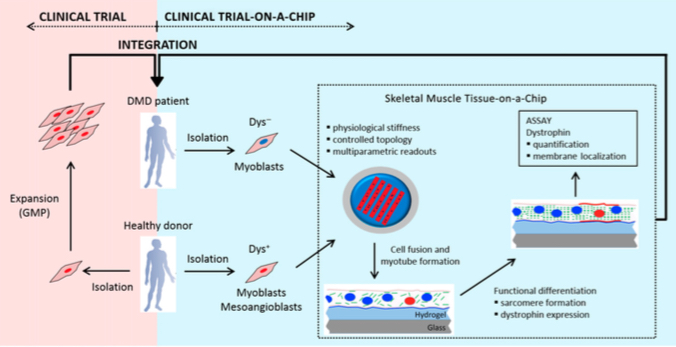 obiettivi che si pongono da anni i ricercatori per combattere la distrofia muscolare di Duchenne. Uno dei punti cruciali, durante gli studi preclinici e clinici, è quantificare la produzione di nuova distrofina funzionante e valutare se i livelli siano sufficienti per arrestare la degenerazione muscolare. Tutta una serie di studi indicano che il 30% di produzione di distrofina potrebbe bastare per contrastare la Duchenne, ma i dati accumulati negli ultimi anni hanno mostrato che i livelli di distrofina prodotta sono molto variabili, a seconda degli approcci terapeutici e delle condizioni dei trial, e purtroppo spesso insufficienti.
obiettivi che si pongono da anni i ricercatori per combattere la distrofia muscolare di Duchenne. Uno dei punti cruciali, durante gli studi preclinici e clinici, è quantificare la produzione di nuova distrofina funzionante e valutare se i livelli siano sufficienti per arrestare la degenerazione muscolare. Tutta una serie di studi indicano che il 30% di produzione di distrofina potrebbe bastare per contrastare la Duchenne, ma i dati accumulati negli ultimi anni hanno mostrato che i livelli di distrofina prodotta sono molto variabili, a seconda degli approcci terapeutici e delle condizioni dei trial, e purtroppo spesso insufficienti.
Esistono diversi modi per aumentare l’efficacia di una strategia ma non è possibile sviluppare un trial clinico per ognuno di essi. Come tutti sappiamo i trial sono uno step decisivo per l’approvazione di una nuova terapia ma sono anche molto dispendiosi sia in termini di soldi che in termini di tempo e fatica (non solo per ricercatori e industria ma anche per i pazienti). Sarebbe quindi molto utile avere a disposizione uno strumento propedeutico alla pianificazioni di nuovi studi clinici, che possa testare tutta una serie di variabili e dare precise informazioni sull’efficacia di una strategia prima di provarla sui pazienti. Ed è proprio da quest’idea che è nato il concetto di “clinical trial on a chip”. Si tratta di un innovativo modello di studio in vitro, basato sugli ultimi progressi della microingegneria per lo sviluppo di organi 3-D e di tessuti in microscala, progettato per la valutazione di nuovi farmaci. In poche parole un nuovo strumento hi-tech, piccolo, economico e rapido che mima gli studi clinici sui pazienti.
Nell’ambito degli studi sui processi fisiologici e patologici del tessuto muscolare scheletrico, interessanti ricerche basate sulla microingegneria sono state condotte da un gruppo di ricerca guidato da Nicola Elvassore, del Dipartimento di Ingegneria Industriale dell’Università di Padova. Nel 2010 i ricercatori italiani hanno messo a punto un modello in vitro su “chip” per lo sviluppo e il differenziamento dei miotubi, le unità funzionali del tessuto muscolare scheletrico. Su questo “chip”, costituito da un substrato polimerico e che comprende anche stimoli meccanici e topologici, i mioblasti (le cellule muscolari) sono in grado di proliferare e differenziare in miotubi che producono correttamente la distrofina (sia per quantità sia per distribuzione nella membrana) e che mimano la situazione fisiologica in vivo delle fibre muscolari mature. Inoltre, partendo da mioblasti prelevati da pazienti DMD, i ricercatori sono riusciti a riprodurre lo sviluppo di miotubi con la mutazione genetica responsabile della Duchenne. Un prezioso modello in vitro per lo studio della patologia.
Nell’ultimo studio, pubblicato ad agosto sulla rivista Stem Cells Translational Medicine, il team di Padova – in collaborazione con Giulio Cossu e Francesco Saverio Tedesco – ha utilizzato il modello di “clinical trial on a chip” per testare la terapia cellulare basata sui mesoangioblasti come strategia terapeutica attualmente in studio per la DMD. I mesoangioblasti sono particolari cellule staminali, associate ai vasi sanguigni, identificate e caratterizzate da Giulio Cossu nel 2002 come cellule capaci di rigenerare il tessuto muscolare danneggiato e ripristinare la sua funzionalità. Gli studi di Cossu hanno condotto nel 2011 al primo trial clinico con mesoangioblasti da donatore immunologicamente compatibile in 5 pazienti Duchenne, studio che si è dimostrato sicuro ma poco efficace.
Nello specifico, i ricercatori hanno testato la capacità che hanno i mesoangioblasti umani di ripristinare una corretta produzione e distribuzione della distrofina in mioblasti con una mutazione per la DMD (che non esprimono la proteina). Gli esperimenti sono stati condotti mettendo sul “chip” mioblasti “distrofici” in co-coltura con mesoangioblasti o mioblasti “sani”, con un rapporto di cellule sane:distrofiche di 1:9. Una volta formate le fibre muscolari (i miotubi) è stata valutata la produzione di distrofina. I risultati hanno mostrato che sia i mioblasti sia i mesoangioblasti inducono un ripristino dell’espressione della distrofina nei miotubi DMD. Ma, i mesoangioblasti mostrano un’efficienza nettamente superiore ai mioblasti: in termini numerici si ha rispettivamente un 40% di distrofina prodotta rispetto a un 15%. Per quello che riguarda la distribuzione, con la co-coltura di mesoangioblasti la distrofina è localizzata lungo tutto il miotubo. Il 40% di produzione di distrofina è un dato importante perché supera quella soglia del 30% che la comunità scientifica ritiene come necessaria per avere un effetto terapeutico.
Questo studio è molto interessante per due principali motivi: prima di tutto è decisamente innovativo ed è un apripista per l’utilizzo del metodo “trial on a chip” e della microingegneria in generale nel campo della Duchenne (un altro interessante studio per la DMD basato sulla microingegneria è quello pubblicato da Marco Quarta di cui Parent Project Onlus ha parlato qui e qui, in secondo luogo fornisce risultati favorevoli alla possibile efficacia della terapia cellulare basata sui mesoangioblasti. Un incoraggiamento quindi a proseguire su questa via, nonostante i deboli dati di efficacia riscontrati nello studio clinico, e che pone le basi per valutare e testare tutta una serie di variabili che possono influenzare ed essere determinanti per l’efficacia della terapia cellulare.
La comunità scientifica si è così dotata di un’arma in più per continuare la battaglia contro la Duchenne. I punti di forza di questo nuovo approccio “clinical trial on a chip” consistono nella sua semplicità, rapidità ed economicità per testare nuovi farmaci o strategie terapeutiche e, soprattutto, nella possibilità di dare preziose informazioni per la pianificazione dei trial sui pazienti.
Dona ora!
Per un futuro di qualità e un mondo con una cura per la distrofia muscolare di Duchenne e Becker.
Notizie correlate
2 Feb 2024
SRP-5051: positivi i risultati della parte B dello studio clinico MOMENTUM
L’azienda statunitense Sarepta Therapeutics ha diffuso nel comunicato stampa del 29 gennaio i risultati positivi della parte B dello studio clinico…
29 Gen 2024
Le motivazioni dell’EMA sul parere in merito a Translarna
Riportiamo a seguire una sintesi delle motivazioni che hanno portato al parere negativo del comitato dell’EMA in merito a Translarna. La notizia…
26 Gen 2024
Negativo il parere di EMA su Translarna
Con grande amarezza condividiamo la notizia del parere negativo del comitato dell’EMA chiamato a decidere rispetto al rinnovo dell'autorizzazione…
In Evidenza
28 Apr 2026
Accesso a givinostat: stato dell’arte sulla prescrivibilità
La notizia della pubblicazione in Gazzetta Ufficiale della rimborsabilità per givinostat (Duvyzat) per il trattamento della distrofia muscolare di…



