Inibizione farmaco mediata dell’Nfix come nuova terapia per la Distrofia Muscolare di Duchenne
Titolare del progetto: Graziella Messina, Università degli Studi di Milano
Durata: 2 anni
Importo: 20.000 euro
Progetto finanziato da Parent Project aps
Il progetto di ricerca si propone di rallentare la rigenerazione muscolare favorendo un accumulo di fibre muscolari con un metabolismo ossidativo, inducendo complessivamente un miglioramento morfologico e funzionale del muscolo distrofico. Un principio innovativo rispetto alla strategia di aumento rigenerazione. L’idea del team di ricerca è quella di non aumentare ma di rallentare la rigenerazione muscolare, recuperando alcuni studi che avevano già evidenziato come le fibre muscolari che si contraggono lentamente (fibre lente) fossero quelle che degeneravano più tardi nei pazienti.
Le distrofie muscolari sono un gruppo di malattie eterogenee caratterizzate dalla perdita progressiva di tessuto muscolare. Allo stato attuale, i corticosteroidi rappresentano l’unica opportunità terapeutica in grado di ritardare la progressione della patologia. Sebbene la maggior parte degli studi in corso siano focalizzati sulla stimolazione del processo rigenerativo e dell’aumento della massa muscolare, la loro applicabilità clinica potrebbe essere fortemente limitata. E’ noto che le fibre muscolari che si contraggono lentamente (fibre lente) sono quelle che degenerano più tardi nei pazienti DMD. Il muscolo distrofico è un tessuto strutturalmente fragile e, forzarlo a rigenerarsi e quindi a lavorare di più, potrebbe portare, paradossalmente, a un aggravamento del fenotipo.
Il gruppo di ricerca della Professoressa Messina ha dimostrato che l’assenza del fattore di trascrizione Nfix, Nuclear Factor One, rallenta la rigenerazione e converte tutte le fibre muscolari a fibre a contrazione lenta.
Nei modelli murini distrofici infatti l’assenza di Nfix rallenta la rigenerazione muscolare favorendo un accumulo di fibre muscolari con un metabolismo ossidativo, inducendo complessivamente un miglioramento morfologico e funzionale del muscolo distrofico. Avendo inoltre caratterizzato i processi molecolari che controllano l’espressione di Nfix, l’obiettivo attuale del gruppo della professoressa Messina, è testare un approccio farmacologico basato su due composti per valutarne la capacità di inibizione di Nfix e il loro effetto preliminare sul fenotipo distrofico.
Lavorando con modelli murini distrofici e incrociandoli con il topo privo di Nfix – ribattezzato dal gruppo di ricerca “topo maratoneta” – è stato dimostrato che in assenza di questa proteina il muscolo distrofico è preservato dai diversi segni della patologia, con un miglioramento dei parametri morfologici, una riduzione della fibrosi e dell’infiammazione, fino al recupero della funzionalità muscolare.
Il gruppo di ricerca mira a utilizzare un enzima, la chinasi ERK, che se inibito può bloccare Nfix. In particolare, due antagonisti di ERK, Trametinib (GSK) e Cobimetinib (Roche), sono stati approvati dalla FDA e dall’EMA per il trattamento dei tumori umani, fornendo l’idea per lo sviluppo di un trattamento terapeutico delle distrofie. L’obiettivo principale di questo progetto è quindi quello di valutare l’efficacia di questi due farmaci nell’inibire l’espressione Nfix in due modelli murini distrofici (Sgca-null/mdx-4cv).
Approfondimento
Primo Report
REPORT DEL PRIMO ANNO DEL PROGETTO DI RICERCA INIBIZIONE FARMACOLOGICA DEL FATTORE DI TRASCRIZIONE NFIX: UNA NUOVA PROSPETTIVA TERAPEUTICA PER LE DISTROFIE MUSCOLARI
Finanziato da Parent Project aps, il progetto coordinato da Graziella Messina è uno dei quattro che ha ricevuto, attraverso il bando per la ricerca 2018, la tipologia di finanziamento detta Fast Track di importo di 20.000€. Il progetto è iniziato a febbraio del 2019 e ha una durata di due anni. L’idea innovativa del team di ricerca è quella di rallentare la rigenerazione muscolare favorendo un accumulo di fibre muscolari con un metabolismo ossidativo, inducendo complessivamente un miglioramento morfologico e funzionale del muscolo distrofico
I processi molecolari alla base dell’insorgenza e progressione delle distrofie muscolari non sono ancora completamente noti. Sebbene si conoscano i geni e le mutazioni che causano la patologia, la distrofia muscolare di Duchenne è una malattia eterogenea, nella quale diversi aspetti (come infiammazione, rigenerazione/degenerazione muscolare, tipologia dei muscoli interessati) compartecipano nel determinare il quadro diagnostico e prognostico. Comprendere questa complessità e i fattori coinvolti nella malattia consentirà di aumentare l’efficienza delle future terapie cellulari e geniche in corso di sviluppo.
Il fattore di trascrizione Nfix (Nuclear Factor One) è una delle proteine coinvolte nella progressione della distrofia muscolare di Duchenne. Nel nostro laboratorio è stato dimostrato che l’assenza di Nfix a livello genetico in topi distrofici determina un miglioramento sia fisiologico sia funzionale dei muscoli: minore infiammazione, minore degenerazione muscolare, minore fibrosi, migliore prestazione fisica.
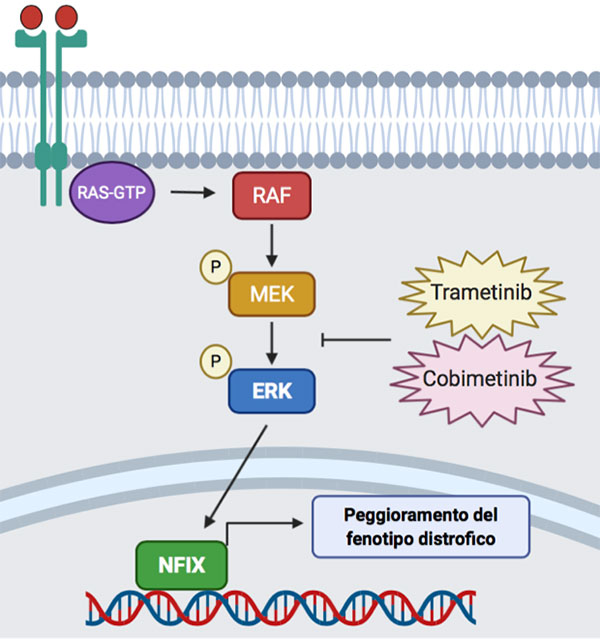
Slide progetto ‘Inibizione farmaco mediata dell’Nfix come nuova terapia per la Distrofia Muscolare di Duchenne’ di Graziella Messina
Qualche anno dopo, abbiamo scoperto una delle vie di segnalazione che regola i livelli del fattore Nfix: durante lo sviluppo e le fasi post-natali delle cellule muscolari, Nfix è regolato positivamente dalle MAP chinasi, in particolare dall’enzima ERK.
Da qui l’idea di inibire Nfix attraverso l’inibizione farmacologica di ERK.
Durante questo primo anno, abbiamo testato due inibitori di ERK, i farmaci Trametinib (GSK) e Cobimetinib (Roche), utilizzati già in clinica per il trattamento del melanoma metastatico e approvati dalla FDA e dall’EMA.
Inizialmente, abbiamo testato diverse concentrazioni dei due farmaci su colture cellulari di mioblasti primari in vitro. A diverse concentrazioni di Trametinib abbiamo osservato una riduzione sia di p-ERK (ERK attivo) che di Nfix. Il Cobimetinib è in fase di valutazione.
In seguito a tali risultati preliminari, abbiamo scelto il Trametinib e abbiamo condotto i primi esperimenti in vivo: abbiamo somministrato a topi adulti distrofici (topi Sgcanull), per via orale, tre concentrazioni diverse del farmaco (0.3 – 3 – 6 mg/kg) tutti i giorni per 14 giorni. Gli animali trattati sono stati in buona salute e non hanno presentano evidenti effetti collaterali associati al trattamento: il peso dei topi trattati non è variato rispetto al gruppo di controllo. Analizzando il tibiale anteriore dei topi trattati e controllo, abbiamo osservato che 3 e 6 mg/kg di Trametinib determinano una buona riduzione sia di p-ERK che di Nfix (circa il 20%) nei muscoli trattati.
Per capire se tale riduzione dei livelli di Nfix sia sufficiente per ottenere un miglioramento istologico del muscolo distrofico, stiamo completando le analisi sulla morfologia del tessuto calcolando i livelli di rigenerazione e degenerazione muscolare, il calibro delle miofibre, l’estensione delle aree di infiammazione e fibrosi. Una volta raccolti questi dati, valuteremo negli animali trattati la funzionalità muscolare e l’istologia di altri organi (come fegato e reni) responsabili del metabolismo ed escrezione del farmaco.
Report Finale
INIBIZIONE DEL FATTORE DI TRASCRIZIONE NFIX FARMACO-MEDIATA COME NUOVA TERAPIA PER LA DISTROFIA MUSCOLARE DI DUCHENNE – REPORT FINALE
Finanziato da Parent Project aps, il progetto coordinato da Graziella Messina è uno dei quattro che ha ricevuto, attraverso il bando per la ricerca 2018, la tipologia di finanziamento detta Fast Track per l’importo di 20.000€. Il progetto è iniziato a febbraio del 2019 e ha avuto una durata di due anni. L’idea innovativa a cui si è dedicato il team di ricerca è stata quella di rallentare la rigenerazione muscolare favorendo un accumulo di fibre muscolari con un metabolismo ossidativo, note per essere più resistenti ai danni associati alla patologia. Il gruppo di ricerca della Professoressa Messina ha dimostrato che l’assenza del fattore di trascrizione Nfix, Nuclear Factor One, rallenta la rigenerazione e converte tutte le fibre muscolari a fibre a contrazione lenta.
I processi molecolari alla base dell’insorgenza e progressione delle distrofie muscolari non sono ancora completamente noti. Sebbene se ne conoscano le basi genetiche, la distrofia muscolare di Duchenne è una patologia complessa, nella quale diversi aspetti (come infiammazione, rigenerazione/degenerazione muscolare, tipologia dei muscoli interessati) compartecipano nel determinare il quadro diagnostico e di progressione. Comprendere questa complessità e i fattori coinvolti nella patologia consentirà di aumentare l’efficienza delle future terapie cellulari e geniche in corso di sviluppo.
Il fattore di trascrizione Nfix (Nuclear Factor One) è una delle proteine responsabili della progressione della distrofia muscolare di Duchenne. Nel laboratorio della Professoressa Messina è stato dimostrato che l’assenza di Nfix a livello genetico in topi distrofici determina un miglioramento sia fisiologico sia funzionale dei muscoli: minore infiammazione, minore degenerazione muscolare, minore fibrosi, migliore prestazione fisica.
L’obiettivo del gruppo di ricerca è stato quello di sviluppare un approccio farmacologico per inibire la proteina Nfix e ottenere un miglioramento istologico e funzionale nella distrofia muscolare di Duchenne.
Per inibire farmacologicamente una proteina è necessario conoscere bene quali sono i circuiti molecolari che la regolano nelle cellule, per poi potere interferire con essi dall’esterno.
Qualche anno fa, il gruppo di ricerca ha scoperto una delle vie di segnalazione che regolano i livelli del fattore Nfix nelle cellule muscolari: durante lo sviluppo e le fasi post-natali dei mioblasti, Nfix è regolato dalle MAP chinasi, in particolare dall’enzima ERK.

Slide progetto ‘Inibizione farmaco mediata dell’Nfix come nuova terapia per la Distrofia Muscolare di Duchenne’ di Graziella Messina
Grazie al contributo di Parent Project aps, il team ha deciso di indagare circa il possibile riutilizzo nella Duchenne del farmaco Trametinib (GSK) – già utilizzato in clinica per il trattamento del melanoma metastatico – in grado di inibire le MAP chinasi e ridurre l’attività dell’enzima ERK. Somministrando questo farmaco prima in culture cellulari in vitro e poi in un modello distrofico, il Sarcoglicano null, è stato osservato un buon livello di inibizione di Nfix. In particolare, topi distrofici adulti (topi Sgca null) trattati con il Trametinib per via orale tutti i giorni per 14 giorni a due dosi diverse (3 e 6 mg/kg) hanno mostrato una buona riduzione di Nfix (circa il 20%) nei muscoli rispetto al controllo.
Inoltre, i muscoli trattati con Trametinib presentavano un maggior numero di fibre muscolari lente a metabolismo ossidativo, note per essere più resistenti ai danni associati alla patologia. Tuttavia, per gli altri parametri morfologici muscolari analizzati (calibro delle miofibre, livelli di rigenerazione e necrosi, estensione aree di infiammazione, fibrosi) i ricercatori non hanno riscontrato dei cambiamenti significativi rispetto al gruppo controllo, ai dosaggi e tempistiche seguiti.
In modo completamente inatteso hanno, purtroppo, notato l’aumento di calcificazioni muscolari in seguito al trattamento con il farmaco. Hanno riscontrato tali alterazioni istologiche soltanto nei topi distrofici trattati e non in topi sani (wild-type) a cui sono stati somministrati gli stessi dosaggi di Trametinib alle stesse tempistiche.
Le calcificazioni muscolari indotte dal trattamento cronico del Trametinib non erano state mai descritte finora per il farmaco, i cui trial pre-clinici e clinici precedenti (necessari per il suo utilizzo in clinica) sono stati condotti su modelli animali e volontari/pazienti non affetti da distrofia muscolare di Duchenne.
Questo aspetto ha chiaramente rappresentato un ostacolo all’ulteriore sviluppo dello studio, limitando la possibilità di aumentare il dosaggio e/o le tempistiche di somministrazione del Trametinib che è in grado di diminuire Nfix nei muscoli distrofici in maniera non sufficiente a ottenere il miglioramento istologico sperato.
I risultati di questo progetto, sebbene non completamente positivi, hanno permesso di fare luce sulla regolazione di Nfix da parte delle MAPK ed ERK in un contesto distrofico.
Ciò consentirà di approfondire il legame tra ERK ed Nfix, riuscendo a trovare una interazione più diretta e testare farmaci sempre più specifici. Inoltre, in un processo di pura serendipity, tale correlazione tra ERK, distrofia e calcificazioni muscolari (mai descritta finora) apre le porte a numerose linee di ricerca per la comprensione dei meccanismi molecolari e cellulari alterati nella distrofia muscolare.
